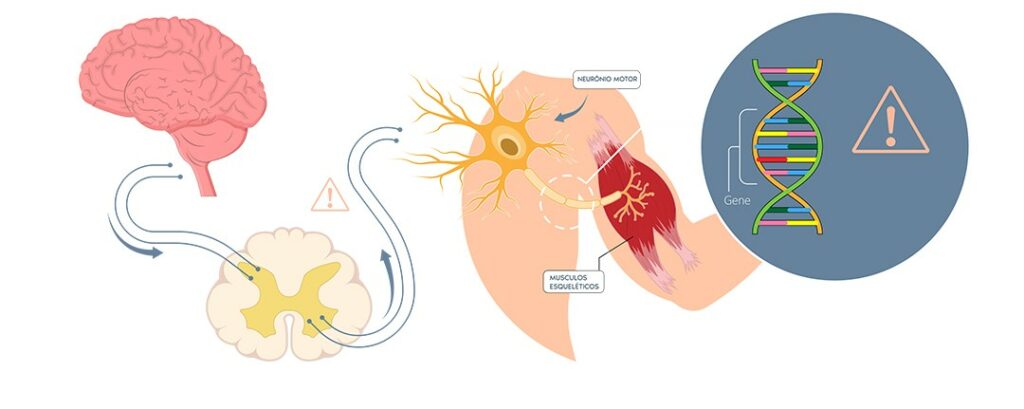
La Atrofia Muscular Espinal (AME) es una enfermedad genética rara, hereditaria y de carácter degenerativo, causada por alteraciones en el gen SMN1 (Survival Motor Neuron 1). Este gen es responsable de la producción de la proteína SMN, esencial para la supervivencia de las neuronas motoras, células encargadas de controlar los movimientos del cuerpo.
Cuando esta proteína está ausente o se encuentra en niveles muy bajos, se produce una degeneración progresiva de las neuronas motoras, lo que provoca debilidad muscular y afecta funciones básicas como respirar, tragar y moverse.
La forma más común y grave de la enfermedad, la AME tipo 1, puede manifestarse en los primeros meses de vida y evolucionar rápidamente si no se inicia un tratamiento. Otras formas, como la AME tipo 2 y la AME tipo 3, varían en gravedad, pero también generan limitaciones motoras significativas a lo largo de la vida.
Cómo ocurre la transmisión genética de la AME
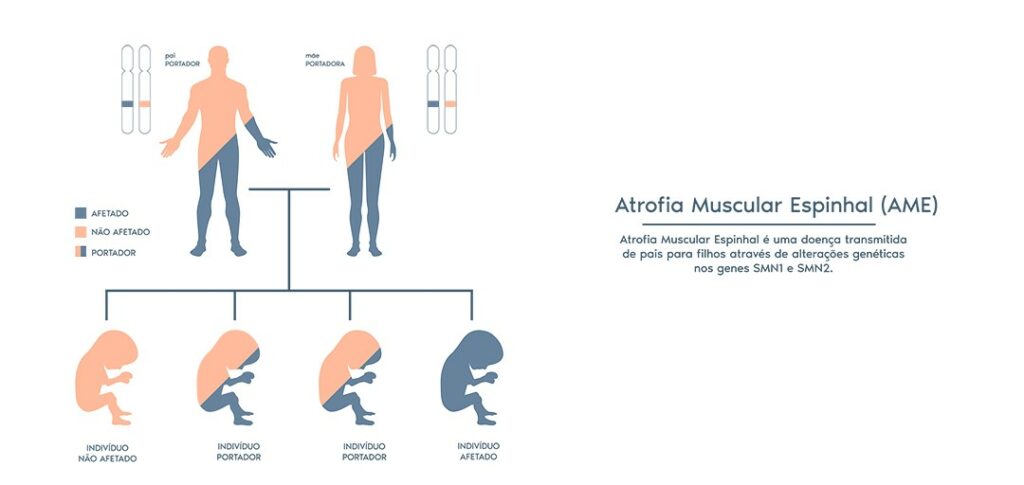
Por ser una condición autosómica recesiva, la AME solo se manifiesta cuando el niño hereda dos copias alteradas del gen —una de cada progenitor—. Así, padres portadores asintomáticos pueden tener hijos con la enfermedad sin presentar ningún síntoma.
En promedio, 1 de cada 40 a 60 personas es portadora de una mutación en el gen SMN1. Cuando dos portadores tienen hijos, existe un 25% de probabilidad de que el niño herede ambas copias alteradas y desarrolle AME, un 50% de probabilidad de ser solo portador y un 25% de probabilidad de nacer sin alteraciones en el gen.
Esta estadística demuestra cómo muchas enfermedades genéticas pueden permanecer “invisibles” durante generaciones, hasta que dos portadores coinciden.
Prueba genética para AME: el papel del CGT en la planificación reproductiva
Hoy en día es posible identificar el riesgo de transmitir enfermedades como la AME incluso antes del embarazo, a través del Test de Compatibilidad Genética (CGT).
Este análisis estudia el ADN de ambos miembros de la pareja e identifica si comparten mutaciones en los mismos genes asociados a enfermedades genéticas recesivas, como AME, fibrosis quística, síndrome del X frágil o beta talasemia, entre otras.
La recolección es sencilla, generalmente a partir de una muestra de sangre o saliva, y utiliza la tecnología de secuenciación de nueva generación (NGS), capaz de examinar cientos de genes de forma simultánea con alta precisión.
Si la pareja resulta portadora de las mismas variantes, el asesoramiento genético orienta sobre las opciones disponibles para reducir el riesgo de transmisión. Entre ellas, se destaca el uso del PGT-M (Test Genético Preimplantacional para Enfermedades Monogénicas).
Cómo funciona el PGT-M: prevención antes del embarazo
Durante un tratamiento de Fertilización in Vitro (FIV), el PGT-M permite analizar el ADN de una pequeña muestra (biopsia) del embrión antes de ser transferido al útero. De esta manera, es posible seleccionar embriones que no presenten las variantes genéticas familiares de riesgo.
Susana, asesora científica de Igenomix en América Latina, parte del Vitrolife Group, explica que es posible seleccionar un embrión que no presente las variantes genéticas familiares de riesgo. Además, mediante la misma biopsia embrionaria, realizar el estudio para detectar alteraciones cromosómicas fuertemente relacionadas con pérdidas gestacionales o fallos de implantación.
Aunque la prueba para AME es ampliamente utilizada, requiere el desarrollo de una sonda personalizada, diseñada específicamente para cada familia a partir del ADN de los futuros padres. Esto garantiza precisión y seguridad en la identificación de los embriones sanos.
Curiosidades sobre la Atrofia Muscular Espinal y la genética
• El gen SMN2, “hermano” del SMN1, también está presente en nuestro ADN. Produce pequeñas cantidades de la proteína SMN y puede influenciar la gravedad de la AME. Cuantas más copias del SMN2 tenga una persona, más leve tiende a ser la forma de la enfermedad.
• El tamizaje neonatal para AME ya es una realidad en varios países, permitiendo el diagnóstico poco después del nacimiento y el inicio temprano del tratamiento, lo que mejora significativamente el pronóstico.
• En los últimos años, nuevas terapias génicas han comenzado a transformar el panorama de la AME, ofreciendo tratamientos dirigidos a la causa genética de la enfermedad , un avance que refuerza el valor de la medicina de precisión.
• Conocer si se es portador antes del embarazo es una forma de prevención genética que permite tomar decisiones informadas y preservar la autonomía reproductiva de la pareja.
Decisiones conscientes y medicina de precisión
El avance de las pruebas genéticas ha ampliado el acceso a la prevención de enfermedades hereditarias y ha traído nuevas posibilidades para quienes desean tener hijos de forma segura.
Conocer el propio ADN permite planificar el futuro con mayor claridad, siendo una de las maneras más poderosas de cuidar de la próxima generación.
En el caso de que el CGT identifique un alto riesgo para una enfermedad, es posible evitar la transmisión a la descendencia por medio del estudio genético PGT-M, que requiere una Fecundación in Vitro (FIV) para que sea posible identificar el embrión libre de la enfermedad antes del embarazo.
La combinación entre el CGT (para detectar riesgos genéticos en los padres) y el PGT-M (para analizar embriones) es actualmente una de las estrategias más seguras para prevenir enfermedades hereditarias graves, ofreciendo a las familias la posibilidad de interrumpir la transmisión de mutaciones genéticas.
El CGT y el PGT-M son herramientas que ayudan a las parejas en la planificación familiar y en la prevención de enfermedades genéticas.